Descripción general de la inmunidad adaptativa
El sistema inmunológico adaptativo está compuesto por células y procesos sistémicos altamente especializados que eliminan o previenen el crecimiento patógeno.
OBJETIVOS DE APRENDIZAJE
Describe la inmunidad adaptativa
CONCLUSIONES CLAVE
Puntos clave
- La respuesta inmune adaptativa proporciona al sistema inmune de los vertebrados la capacidad de reconocer y recordar patógenos específicos para generar inmunidad y montar ataques más fuertes cada vez que se encuentra el patógeno.
- Las células del sistema inmunológico adaptativo son un tipo de leucocito llamado linfocito. Las células B y las células T son los principales tipos de linfocitos implicados en la inmunidad adaptativa.
- Las células B y T pueden crear células de memoria para defenderse de futuros ataques del mismo patógeno al montar una respuesta inmune adaptativa más fuerte y rápida contra ese patógeno antes de que pueda causar síntomas de infección.
- Las células que presentan antígenos presentan antígenos capturados a linfocitos inmaduros, que luego maduran para ser específicos de ese antígeno y trabajan para destruir patógenos que expresan ese antígeno.
- Los trastornos de hipersensibilidad (alergias) pueden ocurrir cuando se forma una respuesta inmune adaptativa contra antígenos que no están asociados con patógenos, como el polen. Los trastornos de hipersensibilidad más complejos pueden involucrar a las células T citotóxicas y causar inflamación crónica y daño a los propios tejidos del cuerpo.
Términos clave
- antígeno : Sustancia que induce una respuesta inmunitaria, generalmente una molécula que se encuentra en un patógeno, como una toxina o molécula expresada por el patógeno o las células infectadas por el patógeno.
- hipersensibilidad : trastorno en el que una respuesta inmune adaptativa forma células de memoria específicas para antígenos que no están asociados con patógenos.
- célula presentadora de antígeno : Célula que presenta antígenos capturados a células T inmaduras. Las células dendríticas y los macrófagos son los mejores ejemplos, pero varias otras células también pueden presentar antígenos.
El sistema inmunológico adaptativo, también conocido como sistema inmunológico específico, está compuesto por células y procesos sistémicos altamente especializados que eliminan o previenen el crecimiento patógeno. El sistema inmunológico adaptativo trabaja para proteger y curar el cuerpo cuando falla el sistema inmunológico innato. Proporciona al cuerpo la capacidad de reconocer y recordar patógenos específicos a través de sus antígenos. Este mecanismo permite al sistema inmunológico montar ataques más fuertes cada vez que se encuentra el patógeno, preparándose así para futuros desafíos y previniendo la reinfección por el mismo patógeno.
Funciones del sistema inmunológico adaptativo
El sistema inmunológico adaptativo comienza a funcionar después de que se activa el sistema inmunológico innato. Si una infección progresa a pesar de la inflamación, la fiebre, las células asesinas naturales (NK) y la actividad de los fagocitos del sistema inmunológico innato, se requiere una respuesta más coordinada para destruir el patógeno. La respuesta inmune adaptativa ocurre unos días después de que se inicia la respuesta inmune innata. Las principales funciones del sistema inmunológico adaptativo incluyen:
- El reconocimiento de antígenos específicos “no propios” en presencia de “propios” durante el proceso de presentación de antígenos
- La generación de respuestas que están diseñadas para eliminar al máximo patógenos específicos o células infectadas con patógenos.
- El desarrollo de la memoria inmunológica en el que cada patógeno es “recordado” por un anticuerpo distintivo, que luego puede ser llamado para eliminar rápidamente un patógeno en caso de que ocurran infecciones posteriores.
Formación de inmunidad adaptativa
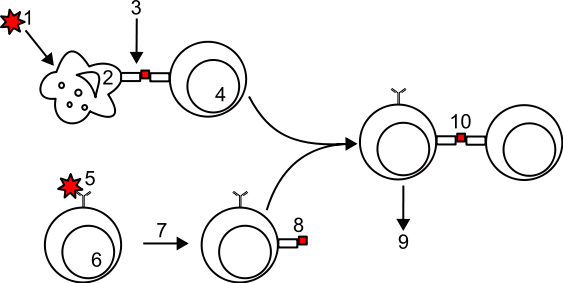
La inmunidad adaptativa se activa cuando un patógeno evade el sistema inmunológico innato durante el tiempo suficiente para generar un nivel umbral de un antígeno. Un antígeno es cualquier molécula que induce una respuesta inmunitaria, como una toxina o un componente molecular de la membrana celular de un patógeno, y es única para cada especie de patógeno. Una respuesta inmune adaptativa típica incluye varios pasos:
- El antígeno del patógeno es captado por una célula presentadora de antígeno (APC), como una célula dendrítica o macrófago, a través de la fagocitosis.
- La APC viaja a una parte del cuerpo que contiene células T y B inmaduras, como un ganglio linfático.
- El antígeno es procesado por la APC y se une a los receptores MHC clase II y a los receptores MHC clase I en la membrana celular de la APC.
- El antígeno se presenta a las células T auxiliares inmaduras y las células T citotóxicas mediante la unión del MHC II (T colaborador) o MHC I (T citotóxico) a los receptores de las células T.
- Estos linfocitos T maduran y proliferan. Las células T auxiliares activan las células B, que proliferan y producen anticuerpos específicos contra el antígeno, mientras que las células T citotóxicas destruyen los patógenos que portan el antígeno que les presentaron las APC.
- Las células de memoria B y T se forman después de que termina la infección.
Presentación de antígenos : la presentación de antígenos estimula a las células T a convertirse en células CD8 + “citotóxicas” o células CD4 + “auxiliares”. Las células citotóxicas atacan directamente a las células que llevan ciertas moléculas extrañas o anormales en sus superficies. Las células T colaboradoras, o células Th, coordinan las respuestas inmunitarias comunicándose con otras células. En la mayoría de los casos, las células T solo reconocen un antígeno si es transportado en la superficie de una célula por una de las moléculas del propio MHC o del complejo principal de histocompatibilidad del cuerpo.
Memoria inmunológica
Cuando se activan las células B y las células T, algunas se convierten en células de memoria. A lo largo de la vida de un animal, estas células de memoria forman una base de datos de linfocitos B y T efectivos. Tras la interacción con un antígeno encontrado previamente, se seleccionan y activan las células de memoria apropiadas. De esta manera, la segunda exposición y las posteriores a un antígeno producen una respuesta inmune más fuerte y rápida. Esto es “adaptativo” porque el sistema inmunológico del cuerpo se prepara para desafíos futuros, que pueden detener una infección por el mismo patógeno antes de que pueda causar síntomas.
La memoria inmunológica puede ser en forma de memoria pasiva a corto plazo o memoria activa a largo plazo. La memoria pasiva suele ser a corto plazo, dura entre unos pocos días y varios meses, y es particularmente importante para los recién nacidos, a quienes se les da memoria pasiva a partir de anticuerpos maternos y células inmunes antes del nacimiento. La inmunidad activa generalmente es a largo plazo y puede adquirirse mediante infección seguida de activación de células B y células T, o adquirirse artificialmente mediante vacunas en un proceso llamado inmunización.
El sistema de memoria tiene algunas fallas. Los patógenos que sufren mutaciones a menudo tienen antígenos diferentes a los conocidos por las células B y T de memoria, lo que significa que diferentes cepas del mismo patógeno pueden evitar la respuesta inmune mejorada por la memoria. Además, la función de las células de memoria permite el desarrollo de trastornos de hipersensibilidad, como alergias y muchas enfermedades crónicas (como esclerosis múltiple o miastenia gravis). En estos casos, las células de memoria se forman para un antígeno que provoca una respuesta inmune sin ser realmente causada por un patógeno, lo que conduce a un daño al cuerpo mediado por el sistema inmunológico debido a actividades e inflamación mediadas por mastocitos, anticuerpos o células T.
Tipos de inmunidad adaptativa
La respuesta inmune adaptativa está mediada por células B y T y crea memoria de inmunidad.
OBJETIVOS DE APRENDIZAJE
Distinguir entre los tipos de inmunidad adaptativa
CONCLUSIONES CLAVE
Puntos clave
- Las células B y las células T, los principales tipos de linfocitos, son muy importantes en el sistema inmunológico adaptativo.
- Las células B, las células T auxiliares tipo 2, los anticuerpos, los mastocitos y los eosinófilos participan en la respuesta inmunitaria humoral.
- Las células T colaboradoras de tipo 1 y las células T citotóxicas participan en la respuesta inmune mediada por células.
- Las células T citotóxicas matan a los patógenos mediante la liberación de perforina, granzimas y proteasas, que hacen que la célula diana sufra apoptosis.
- Los anticuerpos se unen a los patógenos para opsonizarlos, neutralizar las toxinas del patógeno y activar el sistema del complejo del complemento. La IgE también alerta a los mastocitos circulantes y eosinófilos de antígenos conocidos, lo que provoca una rápida respuesta inflamatoria.
Términos clave
- Inmunidad mediada por células : inmunidad adaptativa que no está controlada por anticuerpos y, en cambio, está mediada directamente por las propias células inmunitarias, sobre todo las células T auxiliares tipo 1 y las células T citotóxicas.
- inmunidad humoral : inmunidad adaptativa que se refiere a los componentes específicos de antígeno que fluyen a través del plasma, como los anticuerpos, su función y las células que los producen.
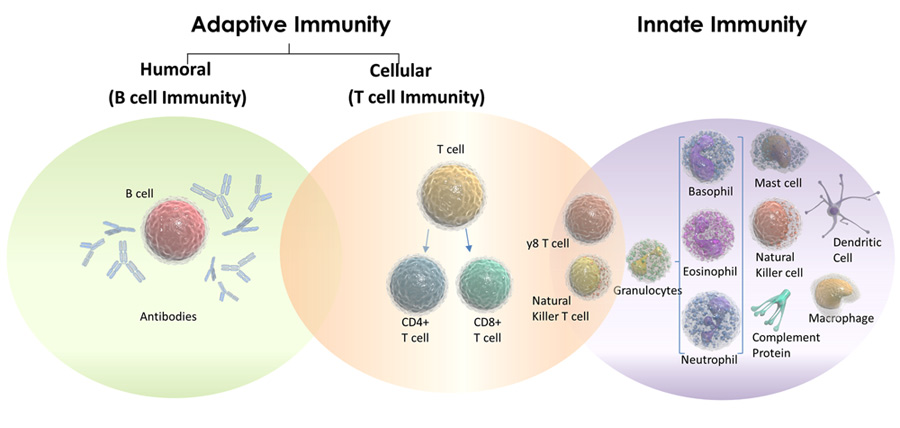
El sistema inmune adaptativo genera una respuesta inmune específica de antígeno más fuerte después de que la respuesta inmune innata falla en prevenir que un patógeno cause una infección. Hay dos subdivisiones del sistema inmunológico adaptativo: inmunidad mediada por células e inmunidad humoral.
Inmunidad mediada por células
La inmunidad mediada por células está controlada por células T auxiliares tipo 1 (T h 1) y células T citotóxicas. Estas células son activadas por células presentadoras de antígenos, lo que hace que maduren rápidamente en formas específicas para ese antígeno. Luego, las células T circulan por el cuerpo para destruir los patógenos de varias formas. Las células T colaboradoras facilitan la respuesta inmune guiando a las células T citotóxicas hacia patógenos o células infectadas con patógenos, que luego destruirán.
Las células T citotóxicas matan a los patógenos de varias formas, incluida la liberación de gránulos que contienen las citotoxinas perforina y granzima, que lisan los pequeños poros de la membrana de un patógeno. Luego, las proteasas producidas por células T ingresan al patógeno e inducen una respuesta de apoptosis dentro de la célula. Las células T colaboradoras secretan citocinas como el interferón-gamma, que pueden activar las células T citotóxicas y los macrófagos.
Inmunidad humoral
La inmunidad humoral se refiere al componente de la respuesta inmune adaptativa que es causado por las células B, los anticuerpos y las células T auxiliares tipo 2 (T h 2), así como los mastocitos circulantes y los eosinófilos en menor grado. Su nombre proviene de la idea de que la sangre es uno de los humores del cuerpo, ya que los anticuerpos proporcionan inmunidad pasiva o activa a través de la circulación en el torrente sanguíneo.
Las células T colaboradoras de tipo 2 se incluyen en el sistema inmunitario humoral porque presentan antígenos a las células B inmaduras, que experimentan una proliferación para volverse específicas del antígeno presentado. Luego, las células B producen rápidamente una gran cantidad de anticuerpos que circulan por el plasma del cuerpo.
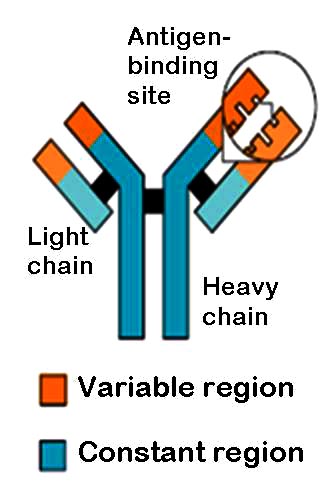
Los anticuerpos proporcionan varias funciones en la inmunidad humoral. Seis clases diferentes de anticuerpos proporcionan funciones distintas e interactúan con diferentes células del sistema inmunológico. Todos los anticuerpos se unen a los patógenos para opsonizarlos, lo que facilita que las células fagocíticas se unan al patógeno y lo destruyan. También neutralizan las toxinas producidas por ciertos patógenos y proporcionan la activación de la vía del complemento, en la que las proteínas circulantes se combinan en una cascada compleja que forma un complejo de ataque de membrana sobre la membrana de una célula patógena, que lisa la célula.
Los mastocitos y los eosinófilos se consideran parte del sistema inmunológico humoral porque pueden sensibilizarse hacia ciertos antígenos a través de la inmunoglobina E (IgE) circulante, un tipo específico de anticuerpo producido por las células B. La IgE se une a los mastocitos y eosinófilos cuando se detecta un antígeno, utilizando un tipo de receptor Fc en el mastocito o eosinófilos que tiene una alta afinidad de unión con IgE. Esta unión provocará la desgranulación y la liberación de mediadores inflamatorios que inician una respuesta inmune contra el antígeno. Este proceso es la razón por la que las células B de memoria pueden causar la formación de hipersensibilidad (alergia), ya que la IgE circulante de esas células de memoria activará una rápida respuesta inflamatoria e inmunitaria.
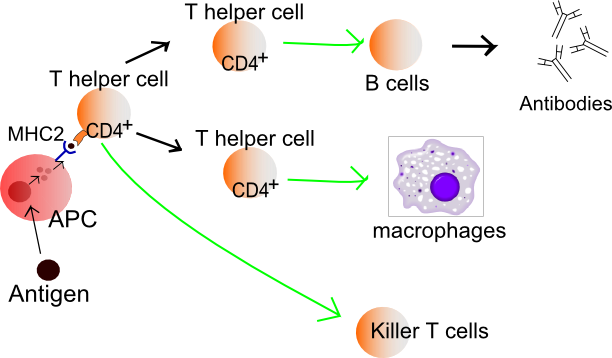
Tipos de inmunidad adaptativa : este diagrama de inmunidad adaptativa indica el flujo del antígeno a APC, MHC2, CD4 +, células T auxiliares, células B, anticuerpos, macrófagos y células T asesinas.
Maduración de las células T
Las células T se originan a partir de células madre hematopoyéticas en la médula ósea y experimentan una selección positiva y negativa en el timo para madurar.
OBJETIVOS DE APRENDIZAJE
Describir la maduración de las células T
CONCLUSIONES CLAVE
Puntos clave
- Los progenitores hematopoyéticos derivados de células madre hematopoyéticas pueblan el timo y se expanden por división celular para generar una gran población de timocitos inmaduros. Una vez que el timo se vuelve inactivo más adelante en la vida, las células T inmaduras existentes proliferarán a través de la expansión clonal.
- Aproximadamente el 98% de los timocitos mueren durante los procesos de desarrollo en el timo al fallar la selección positiva o la selección negativa, mientras que el otro 2% sobrevive y abandona el timo para convertirse en células T inmunocompetentes maduras.
- Durante la selección positiva, solo las células T que pueden unirse al MHC se mantienen vivas. El resto es asesinado por una señal apoptótica para que las células T no funcionales no ingresen al cuerpo y desplacen a las células T funcionales.
- Durante la selección negativa, la mayoría de las células T que se unen con demasiada facilidad a los autoantígenos mueren. Algunas se mantienen vivas y se diferencian en células T reg, que ayudan a prevenir las respuestas inmunes mediadas por células hiperactivas.
- Las enfermedades autoinmunes pueden ser causadas por anticuerpos o células T que pueden unirse a los propios antígenos, causando daño a los propios órganos y tejidos. Pueden deberse a una selección negativa fallida y, a menudo, tienen un componente genético.
Términos clave
- timo : una glándula sin conductos que consta principalmente de tejido linfático primario que es el sitio de maduración y selección de linfocitos.
- selección negativa : proceso mediante el cual se examinan las células T para destruir aquellas que tienen una alta afinidad por unirse a los propios antígenos (y que potencialmente causan autoinmunidad).
- Selección positiva : proceso mediante el cual se examinan las células T de modo que solo se mantengan con vida las que pueden unirse al MHC.
Las células T pertenecen a un grupo de glóbulos blancos conocidos como linfocitos y desempeñan un papel central en la rama mediada por células del sistema inmunológico adaptativo. Se distinguen de otros linfocitos, como las células B y las células asesinas naturales (células NK), por la presencia de un receptor de células T (TCR) en la superficie celular. Las células T se producen en la médula ósea, pero viajan al timo para madurar. Los linfocitos T pueden ser linfocitos T auxiliares o linfocitos T citotóxicos en función de si expresan glicoproteína CD4 (auxiliar) o CD8 (citotóxica).
Maduración de las células T
Todas las células T se originan a partir de células madre hematopoyéticas en la médula ósea, que son capaces de diferenciarse en cualquier tipo de glóbulo blanco. Las células T inmaduras que migran al timo se denominan timocitos. Los primeros timocitos no expresan ni CD4 ni CD8 y, por lo tanto, se clasifican como células doble negativas (CD4-CD8-). A medida que avanzan en su desarrollo, se convierten en timocitos doblemente positivos (CD4 + CD8 +) y finalmente maduran a timocitos positivos simples (CD4 + CD8- o CD4-CD8 +) que se liberan del timo a los tejidos periféricos. Normalmente, estos timocitos maduros todavía se denominan “inmaduros” o “ingenuos” porque no se les ha presentado un antígeno. Viajan a sitios que contienen tejido linfoide secundario, como los ganglios linfáticos y las amígdalas, donde se presentan los antígenos.
El timo aporta menos células a medida que una persona envejece. A medida que su masa funcional se reduce aproximadamente un 3% por año durante la mediana edad, se produce una disminución correspondiente en la producción tímica de células T vírgenes, lo que deja que la expansión clonal de células T inmaduras desempeñe un papel más importante en la protección de los sujetos mayores. Por lo tanto, se cree que el timo es importante en la construcción de una gran reserva de células T vírgenes poco después del nacimiento que luego pueden funcionar sin el apoyo del timo.
Selección positiva de células T
Durante la maduración de los timocitos, el 98% de las células T se descartan por selección, que es un mecanismo diseñado para asegurar que las células T funcionen sin mayores problemas. La selección positiva designa las células T capaces de interactuar con MHC. Los timocitos doblemente positivos (CD4 + / CD8 +) se mueven profundamente en el tejido de la corteza tímica donde se presentan con autoantígenos. Estos son expresados por células epiteliales corticales tímicas que expresan tanto moléculas MHC I como MHC II en la superficie de las células corticales. Solo los timocitos que interactúan con MHC I o MHC II recibirán una “señal de supervivencia” vital. Aquellos que no pueden interactuar sufrirán apoptosis (muerte celular). Esto asegura la funcionalidad de las células T, ya que las células T con receptores no funcionales no pueden recibir antígenos y, por lo tanto, son inútiles para el sistema inmunológico. Si se permitiera la circulación de células T no funcionales, desplazarían a las células T funcionales y ralentizarían la velocidad a la que se forman las respuestas inmunitarias adaptativas. La gran mayoría de los timocitos mueren durante este proceso.
La diferenciación de un timocito en una versión auxiliar o citotóxica también se determina durante la selección positiva. Las células doble positivas (CD4 + / CD8 +) que se seleccionan positivamente en moléculas MHC de clase II eventualmente se convertirán en células T auxiliares CD4 +, mientras que las células seleccionadas positivamente en moléculas MHC de clase I maduran en células T citotóxicas CD8 +. A continuación, el timo indica a la célula AT que se convierta en una célula CD4 + al reducir la expresión de sus receptores de superficie celular CD8. Si la célula no pierde su señal, continuará reduciendo CD8 y se convertirá en una célula positiva única CD4 +. Pero si hay una interrupción de la señal, en su lugar, reducirá las moléculas de CD4, convirtiéndose eventualmente en una sola célula positiva CD8 +. Este proceso no elimina los timocitos que pueden sensibilizarse frente a los autoantígenos, lo que provoca autoinmunidad.
Selección negativa de células T
La selección negativa elimina los timocitos que son capaces de unirse fuertemente a los autoantígenos presentados por el MHC. Los timocitos que sobreviven a la selección positiva migran hacia el límite de la corteza tímica y la médula tímica (la parte del timo donde las células T entran en circulación). Mientras están en la médula, nuevamente se presentan con autoantígeno en complejo con moléculas MHC en células epiteliales tímicas. Los timocitos que interactúan demasiado con el antígeno reciben una señal apoptótica que conduce a la muerte celular.
Sin embargo, algunas células se seleccionan para convertirse en células T-reg, que conservan su capacidad de unirse a autoantígenos con el fin de suprimir las respuestas inmunitarias hiperactivas. Estas células pueden proteger contra la autoinmunidad. Las células restantes salen del timo como células T maduras vírgenes. Este proceso es un componente importante de la tolerancia central, un proceso que previene la formación de células T autorreactivas que son capaces de inducir enfermedades autoinmunes en el huésped. Las enfermedades autoinmunes reflejan una pérdida de tolerancia central en la que las propias células B y T del cuerpo se sensibilizan hacia los autoantígenos. Muchos trastornos autoinmunitarios están mediados principalmente por anticuerpos, pero algunos están mediados por células T. Un ejemplo de lo último es la enfermedad de Crohn, en la que las células T atacan el colon.
Linfocitos
Un linfocito es un tipo de glóbulo blanco en el sistema inmunológico de los vertebrados.
OBJETIVOS DE APRENDIZAJE
Describe el papel de los linfocitos.
CONCLUSIONES CLAVE
Puntos clave
- Los principales tipos de células T son las células T auxiliares, las células T citotóxicas, las células T de memoria y las células T reguladoras.
- Los principales tipos de células B son células plasmáticas, plasmablastos, células B de memoria y células B reguladoras.
- Las células T participan en la inmunidad mediada por células, mientras que las células B son las principales responsables de la inmunidad humoral (relacionada con anticuerpos).
- Si se detecta un antígeno nuevamente después de la respuesta inmune adaptativa inicial, las células T de memoria crean nuevas células T auxiliares y citotóxicas, mientras que las células B de memoria crean nuevos anticuerpos.
- Los linfocitos T y B reguladores suprimen las respuestas inmunitarias al final de una infección y suprimen los linfocitos T y B implicados en la autoinmunidad.
Términos clave
- Células T de memoria : un tipo de célula T que se diferencia rápidamente en células T cooperadoras y citotóxicas si se detecta su antígeno asociado.
- Célula plasmática : tipo de célula B que produce la mayoría de los anticuerpos durante el desarrollo de la respuesta inmunitaria adaptativa.
Un linfocito es un tipo de glóbulo blanco en el sistema inmunológico, que incluye las células B y T del sistema inmunitario adaptativo y las células asesinas naturales (NK) del sistema inmunitario innato.
Las células B y T y sus diversas subdivisiones realizan muchas funciones inmunitarias adaptativas.
Células T
Las células T maduran en el timo y contienen receptores de células T (TCR) que les permiten unirse a los antígenos de los complejos MHC. Las células T son un componente principal de la inmunidad adaptativa mediada por células porque proporcionan una vía para la destrucción directa de patógenos. Hay dos tipos principales de células T que expresan CD4 o CD8, según las señales que ocurren durante la maduración de las células T, así como tipos menos comunes:
- Las células T colaboradoras (CD4) facilitan la organización de las respuestas inmunitarias y pueden unirse al MHC de clase II. Las células T auxiliares del subtipo 2 presentan antígenos a las células B. Las células T auxiliares del subtipo 1 producen citocinas que guían a las células T citotóxicas hacia los patógenos y activan los macrófagos.
- Las células T citotóxicas (CD8) destruyen los patógenos asociados con un
antígeno. Funcionan de manera similar a las células NK al unirse al
MHC de clase I y liberar perforina, granzimas y proteasas para inducir la apoptosis en un patógeno. Son diferentes de las células NK porque solo se unen a
células que expresan su antígeno específico y no son grandes ni granulares como las células NK. - Las células T supresoras (células T-reg) conservan parte de su capacidad para unirse a las propias células. Tienen un efecto inmunosupresor que inhibe la inmunidad mediada por células al final de una respuesta y destruye las células T autoinmunes que no se filtran por selección negativa en el timo.
- Las células T de memoria se crean después de que cede una respuesta inmune adaptativa, reteniendo el antígeno presentado. Proliferan y se diferencian rápidamente en células T auxiliares y citotóxicas que son específicas de ese antígeno en caso de que se detecte nuevamente en el cuerpo.
Si bien estas son las categorías principales de linfocitos T, existen otros subtipos dentro de estas categorías, así como categorías adicionales que no se comprenden completamente.
Células B
Las células B participan en la inmunidad adaptativa humoral, produciendo los anticuerpos que circulan por el plasma. Se producen y maduran en los tejidos de la médula ósea y contienen receptores de células B (BCR) que se unen a los antígenos. Mientras están en la médula ósea, las células B se clasifican mediante selección positiva y negativa de una manera algo similar a la maduración de las células T en el timo, con el mismo proceso de matar las células B que no son reactivas a los antígenos o reactivas a los autoantígenos. Sin embargo, en lugar de apoptosis, las células B defectuosas mueren a través de otros mecanismos, como la deleción clonal. Las células B maduras abandonan el timo y viajan al tejido linfoide secundario, como los ganglios linfáticos.
Durante la presentación de antígenos, las células presentadoras de antígenos primero presentan antígenos a las células T. Luego, las células T auxiliares maduras unen su antígeno a las células B vírgenes a través de BCR. Después de la presentación del antígeno, las células B vírgenes migran juntas a centros germinales dentro del tejido linfoide, donde experimentan una proliferación y diferenciación extensas en diferentes tipos de células B maduras. Algunas de las principales categorías de células B que surgen incluyen:
- Células plasmáticas y células B de larga vida que son la principal fuente de anticuerpos. No tienen la capacidad de proliferar y se consideran diferenciados terminalmente.
- Los plasmablastos son células B de vida corta que se producen al comienzo de una infección. Sus anticuerpos tienen una afinidad de unión más débil que los de las células plasmáticas.
- Las células B reguladoras (células B reg) son células B inmunosupresoras que secretan citocinas antiinflamatorias (como IL-10) para inhibir los linfocitos autoinmunes.
- Las células B de memoria son células B inactivas con la misma BCR que la célula B de la que se diferenciaron. Son específicos del antígeno presentado a ese BCR y secretan rápidamente grandes cantidades de anticuerpos específicos del antígeno para evitar la reinfección si ese antígeno se detecta nuevamente.
Además de la producción de anticuerpos, las células B también pueden funcionar en la presentación de antígenos, aunque no en el grado de macrófagos o células dendríticas. Las células B son importantes para la función inmunológica adaptativa, pero también pueden causar problemas. Las células B autorreactivas pueden causar una enfermedad autoinmune que involucra daño e inflamación inducidos por anticuerpos. Ciertas células B pueden sufrir una transformación maligna en células cancerosas, como el linfoma, en las que se dividen continuamente y forman tumores sólidos.
Células presentadoras de antígenos
La presentación de antígenos es un proceso mediante el cual las células inmunitarias capturan antígenos y luego permiten su reconocimiento por las células T.
OBJETIVOS DE APRENDIZAJE
Describir el papel de las células presentadoras de antígenos.
CONCLUSIONES CLAVE
Puntos clave
- Las células del huésped expresan antígenos “propios” que las identifican como tales. Estos antígenos son diferentes de los de las bacterias (antígenos “no propios”) y de las células huésped infectadas por virus (“desaparecidos”).
- La presentación del antígeno consiste en el reconocimiento del patógeno, la fagocitosis del patógeno o sus componentes moleculares, el procesamiento del antígeno y luego la presentación del antígeno a las células T vírgenes.
- El receptor de células T se limita a reconocer péptidos antigénicos solo cuando se une a moléculas apropiadas del complejo principal de histocompatibilidad (MHC), también conocido en humanos como antígeno leucocitario humano (HLA).
- Las células T colaboradoras reciben antígenos del MHC II en una APC, mientras que las células T citotóxicas reciben antígenos del MHC I.Las células T colaboradoras también presentan su antígeno a las células B. Las células dendríticas, las células B y los macrófagos juegan un papel importante en la respuesta innata , y son las células presentadoras de antígeno primarias (APC).
- Las APC utilizan receptores de tipo toll para identificar PAMPS y DAMP, que son signos de una infección y pueden procesarse en péptidos antigénicos si se fagocitan. La mayoría de las APC no pueden diferenciar entre diferentes tipos de antígenos, como pueden hacerlo las células B y T.
Términos clave
- patrón molecular asociado al daño : signos basados en proteínas o ácidos nucleicos de daño inducido por patógenos. Las proteínas DAMP se pueden fagocitar y procesar para la presentación de antígenos.
- citotóxico : población de células T especializadas en inducir la muerte de otras células.
La presentación de antígenos es un proceso en el sistema inmunológico del cuerpo mediante el cual los macrófagos, las células dendríticas y otros tipos de células capturan los antígenos y luego los presentan a las células T ingenuas. La base de la inmunidad adaptativa radica en la capacidad de las células inmunitarias para distinguir entre las propias células del cuerpo y los patógenos infecciosos. Las células del huésped expresan antígenos “propios” que las identifican como pertenecientes al yo. Estos antígenos son diferentes de los de las bacterias (antígenos “no propios”) o de las células huésped infectadas por virus (“desaparecidos”). La presentación del antígeno consiste en general en el reconocimiento del patógeno, la fagocitosis del patógeno o sus componentes moleculares, el procesamiento del antígeno y luego la presentación del antígeno a células T vírgenes (maduras pero aún no activadas).
Células presentadoras de antígeno
Las células presentadoras de antígeno (APC) son células que capturan antígenos del interior del cuerpo y los presentan a las células T ingenuas. Muchas células del sistema inmunológico pueden presentar antígenos, pero los tipos más comunes son los macrófagos y las células dendríticas, que son dos tipos de leucocitos diferenciados terminalmente que surgen de los monocitos. Ambas APC realizan muchas funciones inmunes que son importantes tanto para la inmunidad innata como para la adaptativa, como eliminar los patógenos sobrantes y los neutrófilos muertos después de una respuesta inflamatoria. Las células dendríticas (CD) se encuentran generalmente en tejidos que tienen contacto con el ambiente externo (como la piel o el epitelio respiratorio) mientras que los macrófagos se encuentran en casi todos los tejidos. Algunos tipos de células B también pueden presentar antígenos, aunque no es su función principal.
Las APC fagocitan patógenos exógenos como bacterias, parásitos y toxinas en los tejidos y luego migran, a través de señales de quimiocinas, a los ganglios linfáticos que contienen células T vírgenes. Durante la migración, las APC experimentan un proceso de maduración en el que digieren los patógenos fagocitados y comienzan a expresar el antígeno en forma de péptido en sus complejos MHC, lo que les permite presentar el antígeno a las células T ingenuas. La fase de digestión de antígenos también se denomina “procesamiento de antígenos” porque prepara los antígenos para la presentación. Este complejo MHC: antígeno es luego reconocido por las células T que pasan a través del ganglio linfático. Los antígenos exógenos generalmente se muestran en las moléculas del MHC de clase II, que interactúan con las células T auxiliares CD4 +.
Este proceso de maduración depende de la señalización de otras moléculas de patrón molecular asociado a patógenos (PAMP) (como una toxina o un componente de una membrana celular de un patógeno) a través de receptores de reconocimiento de patrones (PRR), que son recibidos por receptores tipo Toll en el cuerpo de la DC. También pueden reconocer moléculas de patrón molecular asociado al daño (DAMP), que incluyen proteínas degradadas o ácidos nucleicos liberados de células que sufren necrosis. Los PAMP y DAMPS no se consideran técnicamente antígenos en sí mismos, sino que son signos de presencia de patógenos que alertan a las APC a través de la unión al receptor tipo Toll. Sin embargo, si una DC fagocita un PAMP o DAMP, podría usarse como antígeno durante la presentación del antígeno. Las APC son incapaces de distinguir entre diferentes tipos de antígenos por sí mismas, pero las células B y T pueden hacerlo debido a su especificidad.
Presentación de antígeno
Las células T deben presentar antígenos para realizar funciones del sistema inmunológico. El receptor de células T está restringido a reconocer péptidos antigénicos solo cuando se une a moléculas apropiadas de los complejos MHC en APC, también conocido en humanos como antígeno leucocitario humano (HLA).
Las APC pueden activar varios tipos diferentes de células T, y cada tipo de célula T está especialmente equipada para hacer frente a diferentes patógenos, ya sea que el patógeno sea bacteriano, viral o una toxina. El tipo de célula T activada y, por tanto, el tipo de respuesta generada, depende del complejo MHC al que se une el antígeno-péptido procesado.
Las moléculas de MHC de clase I presentan antígeno a las células T citotóxicas CD8 +, mientras que las moléculas de MHC de clase II presentan antígeno a las células T auxiliares CD4 +. Con la excepción de algunos tipos de células (como los eritrocitos), el MHC de clase I es expresado por casi todas las células huésped. Las células T citotóxicas (también conocidas como TC, células T asesinas o linfocitos T citotóxicos (CTL)) son una población de células T especializadas para inducir la muerte de otras células. El reconocimiento de péptidos antigénicos a través de la Clase I por los CTL conduce a la muerte de la célula diana, que está infectada por virus, bacterias intracitoplasmáticas, o está dañada o disfuncional de otra manera. Además, algunas células T auxiliares presentarán su antígeno a las células B, lo que activará su respuesta de proliferación.